复发或难治性T细胞ALL 通用型BE-CAR7 T细胞可诱导白血病缓解
英国研究者Chiesa等报告,在复发或难治性T细胞急性淋巴细胞白血病(ALL)患者中,通用型的、碱基编辑的、抗CD7嵌合抗原受体(BE-CAR7)T细胞可诱导白血病缓解,从而使大多数患者能够成功接受异体造血干细胞移植。(N Engl J Med. 2026; 394: 152-165.)
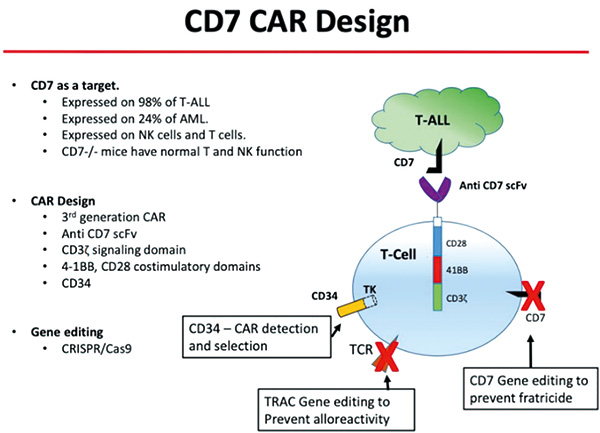
CD7是复发或难治性ALL嵌合抗原受体(CAR)T细胞疗法的理想靶点。此前已有首例人体研究报告了BE-CAR7 T细胞的治疗结果,该BE-CAR7为C→T脱氨介导的、TCRαβ/CD52/CD7三重敲除的制剂。
该项Ⅰ期试验纳入复发或难治性T细胞ALL患儿(≤16岁),先予氟达拉滨、环磷酰胺和alemtuzumab衰竭淋巴细胞,然后给予BE-CAR7 T细胞。有同情救治性(compassionate-use)使用准入途径的成年患者也符合资格。在BE-CAR7 T细胞输注后第28天缓解的患者,随后接受异体造血干细胞移植。主要终点为安全性。次要终点包括缓解期、无病生存期和总生存期。
结果显示,BE-CAR7 T细胞被施用于9例患儿,以及2例有同情救治性使用准入途径的成年患者。淋巴细胞耗竭和BE-CAR7 T细胞输注未导致不可接受的不良事件,所有患者均检测到循环中的CAR7 T细胞。并发症包括1~4级细胞因子释放综合征、短暂性皮疹、多系细胞减少症及机会性感染。
所有患者均在第28天获得了细胞计数未完全恢复的、形态学意义的完全缓解。9例(82%)患者经流式细胞术或聚合酶链式反应分析确认获得深度缓解,得以接受干细胞移植治疗,其中2例量化评估骨髓最小残留病的患者接受了姑息治疗。移植消除了剩余的BE-CAR7 T细胞,并支持供体来源的多系重组。病毒复燃频繁,3例患者在移植后出现有临床意义的病毒相关并发症。
总体而言,接受该试验治疗的11例患者中有7例(64%)在移植后3~36个月内处于持续缓解状态,2例患者有白血病伴CD7表达丧失。 (编译 白婧)














