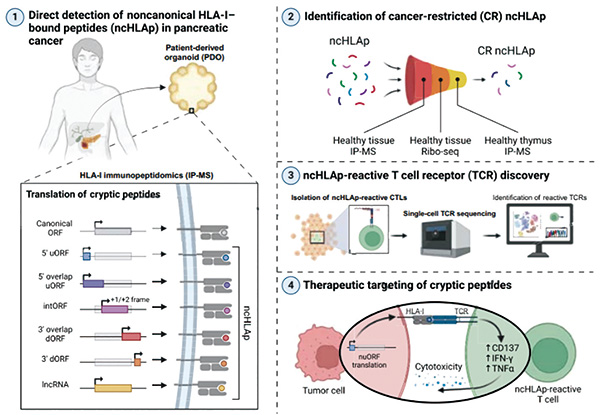
研究揭示胰腺癌隐蔽肽段抗原
美国麻省理工学院Ely等首次系统性地探索了胰腺癌细胞中一类特殊的抗原——隐性抗原肽(cryptic peptides)。研究发现了约500种只存在于胰腺癌肿瘤的隐性抗原肽。胰腺癌细胞异常翻译产生的隐蔽抗原具有癌症特异性、免疫原性和靶向治疗潜力。通过生成靶向抗原肽的T细胞,研究者成功引导T细胞高效清除了胰腺癌细胞,这或许有望为治疗癌王带来全新契机。(Science. 2025年5月8日在线版)
研究者获取了来自胰腺癌患者的肿瘤组织样本,并基于此构建了一批肿瘤类器官。这些类器官能复制、模拟胰腺肿瘤结构以及发育过程。结果显示,随着类器官的生长,组织中产生了大量新生抗原,但绝大多数都属于隐性抗原肽。对胰腺癌患者类器官和肿瘤组织进行深度免疫肽组分析发现,类器官能更精准反映癌细胞特异性肽段。虽然构建了个性化蛋白质基因组数据库,但仅检测到少量突变衍生肽段,而隐蔽肽段检出量超千种。这些肽段源自长链非编码RNA、基因非翻译区、异常阅读框架等非传统区域。研究者从中共鉴定出约1700种隐性抗原肽,平均每个肿瘤类器官中有250种。通过对比包括健康胸腺在内的多种正常组织,筛选出具有癌症特异性的隐蔽肽段。约30%的胰腺癌隐蔽肽段未在正常组织中出现,其中近半数能与常见HLA-A*02:01分子稳定结合。
分析发现,大约有500种隐性抗原肽只存在于胰腺癌细胞而不出现在健康组织中,研究者进一步将这些肽段归类为癌症限制隐性抗原肽。随后,在其中挑选了30多种抗原肽暴露于T细胞环境中。结果有12种抗原肽可以显著刺激T细胞产生特异性的免疫反应。这些被激活的 T 细胞能够识别并杀死表达相应抗原肽的胰腺癌细胞,对正常细胞没有影响。
研究者找到一种增强T细胞的潜在新方向。体外T细胞激活实验显示,癌症特异性隐蔽肽段引发的免疫反应强度与突变新生抗原相当。通过条形码抗原定位技术,成功分离出特异性T细胞受体。借助CRISPR/Cas9技术,将识别这些癌症限制隐性抗原肽的T细胞受体导入到天然T细胞中,构建了一批TCR-T细胞。经基因编辑改造的TCR-T细胞能有效识别肿瘤细胞表面隐蔽抗原,并在体外和动物实验显示,这些TCR-T细胞表现出强大的肿瘤杀伤能力。它们不仅能快速识别目标胰腺癌细胞,还能释放穿孔素、颗粒酶来直接杀死癌细胞,或者分泌干扰素γ、肿瘤坏死因子增强抗肿瘤免疫反应。在胰腺癌小鼠模型中,相较于对照组,TCR-T细胞可显著延缓肿瘤的生长速度。实验组的肿瘤体积更小,同时肿瘤内部含有许多活性较强的TCR-T细胞。这些发现为开发新型细胞免疫疗法提供了关键靶点,特别是针对缺乏有效治疗手段的实体瘤,具有重要临床转化价值。
该研究通过高精度免疫肽检测技术,发现胰腺癌的免疫肽组中富含大量隐蔽肽段。研究发现这些隐蔽肽段有癌症特异性特征,约30%的非常规HLA结合肽具有癌症特异性,其中相当一部分在不同患者间存在共享现象;有免疫激活潜力:在灵敏的体外T细胞激活系统中,癌症特异性隐蔽肽段展现出强劲的免疫激活能力。针对这些肽段设计的T细胞受体改造疗法,在患者来源的胰腺癌类器官模型中成功实现肿瘤杀伤。
相较于直接改造T细胞,研究者认为,未来可以设计一些针对癌症限制隐性抗原肽的疫苗。通过注射疫苗直接刺激,在人体内部“创造”靶向肿瘤的T细胞。该研究首次证实胰腺癌细胞中存在能被免疫系统识别的特异性隐蔽抗原。这些发现为开发新型细胞疗法提供了方向——未来针对胰腺癌乃至其他实体瘤的治疗,可能通过靶向这类“隐形靶点”实现突破。
(编译 韩婧)