转移性结直肠癌患者原发肿瘤部位与贝伐单抗疗效的相关性
背景:转移性结直肠癌患者中,抗血管生成药物贝伐珠单抗依然缺乏有效的疗效预测指标。本研究旨在评估贝伐珠单抗与CAPEOX化疗方案联合一线治疗转移性结直肠癌患者疗效与肿瘤原发部位的相关性。
病人和方法:一个队列由2006至2011年期间来自普通社区的接受CAPEOX联合贝伐珠单抗作为标准一线治疗的667例结肠直癌患者组成,对比贝伐珠单抗获批前,于2003至2006年期间仅接受CAPEOX治疗的213例患者进行比较。主要的观察终点为无进展生存(PFS)和总生存(OS)。采用Kaplan-Meier法绘制生存曲线,log-rank检验比较统计学差异,Cox比例风险模型进行多因素分析。
结果:原发肿瘤位于乙状结肠和直肠的患者接受CAPEOX联合贝伐单抗方案治疗较原发肿瘤位于盲肠至降结肠段的患者无论是PFS(中位PFS 9.3 vs.7.2月;风险比(HR)0.68,95%置信区间0.56-0.82)还是OS(中位OS 23.5 vs.13.0月;风险比(HR)0.47,95%置信区间0.38-0.57)都显著获益。多因素分析调整其他可能的预后因素后进一步证实。然而,在仅接受CAPEOX方案治疗的患者中,原发肿瘤部位与患者的生存未显示相关性。
结论:贝伐珠单抗联合CAPEOX方案一线治疗转移性结直肠癌可能主要使原发肿瘤位于直肠和乙状结肠的患者受益。该假设需要完成的随机临床研究数据进一步验证。
ClinicalTrials.gov编号:NCT00212615
关键词:转移性结直肠癌,贝伐单抗,化疗,原发肿瘤,生物标志物
概述
在全世界范围,结直肠癌是主要的肿瘤相关死亡原因之一[1,2]。在过去的20年中,尽管新的有效的化疗药物和生物制剂如针对血管内皮生长因子(VEGF-A)靶向药物贝伐珠单抗(商品名Avastin®, 罗氏)以及针对表皮生长因子(EGFR)的靶向药物西妥昔单抗和帕尼单抗的应用,使转移性结直肠癌患者的生存有所改善[3-8],转移性结直肠癌患者治疗效果有限仍然是一个主要问题,部分可归因于预测性生物标志物缺乏。KRAS原癌基因突变仍然是目前用于抗EGFR治疗的最佳筛选标记物[9]。贝伐珠单抗用于转移性结直肠癌患者的治疗仍缺乏临床可用的筛选标志[10]。
原发于直肠和近端及远端结肠的肿瘤在大体表现上有差异显著,他们可能存在不同的遗传和表观遗传的改变[11]。贝伐珠单抗的靶点VEGF-A在肿瘤组织的表达水平,也随原发肿瘤部位的而不同,其在远端结肠和直肠癌的表达水平较近端结肠更高[12]。
我们在两个较大的队列中研究了原发肿瘤部位对接受CAPEOX联合或不联合贝伐珠单抗一线治疗转移性结直肠癌患者生存的影响,明确原发肿瘤的部位是否与贝伐珠单抗疗效相关。
方法
病人
组织microRNAs作为生物标记物且接受贝伐珠单抗治疗的结直肠癌临床研究BETmiRC的病例数据纳入分析。本研究回顾性纳入丹麦的10个肿瘤中心在2006-2011年期间一线接受CAPEOXBEV治疗的转移性结直肠患者。这10个站点涵盖了丹麦所有将CAPEOXBEV作为转移性结直肠癌患者首选一线治疗方案之一的所有部门。入选标准包括:经活检证实的结直肠腺癌,接受CAPEOXBEV作为一线全身化疗方案。排除标准包括:同时存在其他恶性肿瘤,组织学为神经内分泌肿瘤,以及CAPEOXBEV方案作为辅助治疗。疗效评估采用计算机断层扫描(CT)及实体瘤疗效评估标准1.0(RECIST 1.0),每三到四个周期对患者进行评效[13]。采用相同的纳入和排除标准,我们建立了接受CAPEOX方案作为一线化疗的另一个队列,并且在该队列中,后续治疗均不包括贝伐珠单抗。这些患者来自Herlev大学医院,来自同期进行的一项临床研究[14]。第二个队列为2003-2006年期间一线接受CAPEOX治疗的结直肠癌患者,而当时在丹麦贝伐单抗并未作为标准一线治疗。给药方式为奥沙利铂 130mg/m^2 第1日静脉滴注,卡培他滨 2000mg/m^2 第1-14天口服±贝伐单抗 7.5mg/kg 第1日静脉滴注,每三周重复。超过98%的患者为高加索人。
数据提取和研究终点
数据从每家医院各患者的病历记录以及采用标准病例报告表方式记录的电子数据库中提取。病理资料和生存数据通过丹麦公民唯一注册系统编号从国家数据库获得。据此,我们能获得所有病理诊断以及病人最新生存状态的完整信息。原发肿瘤部位登记为:(i)盲肠和升结肠(ii)结肠右曲和横结肠 (iii)结肠左曲和降结肠 (iv)乙状结肠和直乙状结肠,或(v)直肠。生存状态更新于2012年11月29日。疾病进展日期定义为根据RECIST 1.0标准,CT评估疾病进展的时间,或者在少数病例中,因患者临床症状恶化,在病历中明确指出为临床进展的日期。研究终点疾病进展时间(PFS)定义为从治疗开始至疾病进展或任何原因引起的患者死亡的时间。距最后一次评效超过3个月死亡且无疾病进展证据的患者,采用其最后确认疾病无进展的评估时间为截点。总生存(OS)定义为从治疗开始至任何原因引起患者死亡的时间。
统计分析
根据病例报告表中的五种分组对原发肿瘤部位进行分类。PFS和OS采用Kaplan-Meier法绘制生存曲线,log-rank检验比较生存曲线差异。Cox比例风险模型分别对PFS和OS进行分析,比较协变量对两队列PFS和OS的影响。随后,我们合并两个队列,采用似然率检验法分析队列间不同肿瘤部位的相互作用。Student的 t检验用于比较平均数和率的差异,Pearson的卡方检验用于比较分布的差异。采用统计软件包R[15]( www.r-project.org) 和 GraphPad Prism5(GraphPad Software, Inc)用于所有的统计分析。所有检验中,P≤0.05认为有统计学意义。
伦理
BETmiRC研究获得当地科学伦理委员会批准(批文号H1-2010-081)。
结果
本研究最终纳入880例患者;667例患者接受CAPEOXBEV治疗,213例患者接受CAPEOX治疗(表1)。原发肿瘤部位在两队列中分布类似,但其他特征两队列间有差异显著。CAPEOXBEV治疗组患者年龄较大,性别女性患者多、PS评分多为0、原发肿瘤未切除以及基线坚持即存在同时性远处转移的患者比例更高。CAPEOXBEV治疗组患者接受一线化疗周期数较CAPEOX治疗组平均多1个周期,但其其后接受伊立替康和西妥昔单抗治疗比例偏少,这有可能是由于随访时间相对短所致。
表1 病例特点
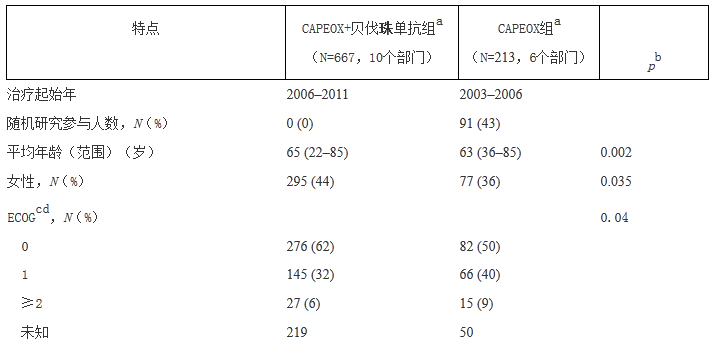
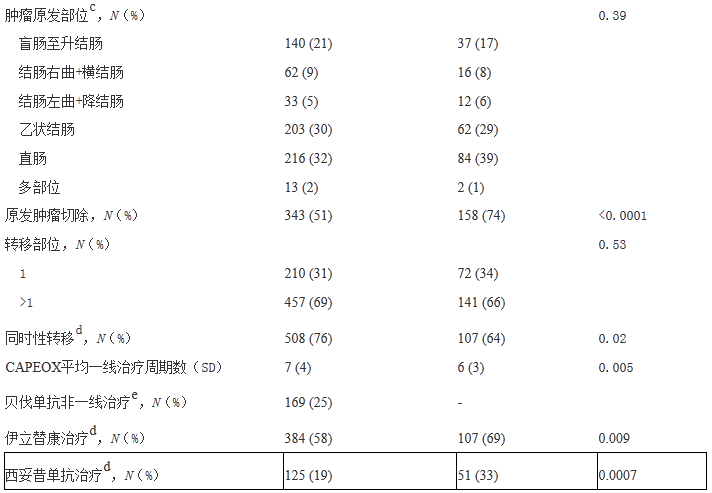
a给药方式为奥沙利铂 130mg/m^2 第1日静脉滴注,卡培他滨 2000mg/m^2 第1-14天口服±贝伐珠单抗 7.5mg/kg 第1日静脉滴注,每三周重复
b Student’s t检验用于比较平均数和率的差异,Pearson’s卡方检验用于比较分布的差异
c由于四舍五入百分比不等于100
d未知变量率的差异未显示,也未进行分布差异检验
e非一线治疗指联合化疗后使用贝伐珠单抗单药或CAPEOX方案后与新的化疗方案联合联合
CAPEOXBEV治疗组患者根据原发肿瘤部位不同明显的分成两个具有显著生存差异的群体(图1)。原发肿瘤位于乙状结肠和直肠的患者较原发肿瘤位于盲肠至降结肠的患者显示出更长的PFS(中位PFS 9.3 vs.7.2月;风险比(HR)0.68,95%置信区间(CI)0.56-0.82)和OS(中位OS 23.5 vs.13.0月;风险比(HR)0.47,95%置信区间(CI)0.38-0.57)。剔除后续治疗中接受西妥昔单抗或伊立替康的病例后OS差异依然存在(补充图S1,见Annals of Oncology 在线版)。
接受CAPEOX方案治疗的患者未显示出与原发肿瘤部位相关的生存差异,中位PFS为6.5 -7.8个月,中位OS为14.1-18.4个月(图1)。该队列中,临床研究和非临床研究的患者在PFS和OS均未显示出统计学差异(数据未显示)。
将患者分为结肠癌和直肠癌亚组后,CAPEOXBEV治疗组中观察到直肠癌患者OS更长(中位OS 24.1 vs.16.6月;HR 0.73,95 %CI 0.61-0.87),而在CAPEOX治疗组无差异(中位OS 14.1vs.16.4月;HR1.02 , 95%CI 0.77-1.35)。
多因素分析显示,经调整潜在预后因素(年龄、性别、原发肿瘤切除、治疗科室、前期辅助化疗、转移部位数目、体力状态评分、白细胞计数及碱性磷酸酶水平)后,CAPEOXBEV治疗组患者不同原发肿瘤部位亚组间生存差异依然存在,而CAPEOX组患者未显示出统计学差异(表2)。剔除缺乏一项或更多潜在预后因子信息的病例并不改变CAPEOXBEV队列中不同原发肿瘤部位分组患者的生存差异(补充表S2,见Annals of Oncology在线版)。
将两队列所有患者按原发肿瘤部位分为两组(盲肠至降结肠与乙状结肠vs.直肠),我们观察到贝伐珠单抗疗效与原发肿瘤部位存在明显相互作用,OS存在显著差异(p=0.004)而PFS无统计学差异(p=0.15)。
讨论
在该探索性分析中,我们提供了转移性结直肠癌原发肿瘤部位与贝伐珠单抗疗效有关或可能存在相互作用的证据。研究数据来自丹麦接受相同标准治疗的队列。对不同肿瘤原发部位进行分层分析,CAPEOXBEV治疗队列可明显分成两个预后组:由原发肿瘤位于盲肠至降结肠组成的较差预后组和由原发肿瘤位于乙状结肠和直肠的较好预后组。多因素分析调整潜在预后影响因子后,这种差异依然存在。而在接受不含贝伐珠单抗的CAPEOX治疗队列中,原发肿瘤部位与生存结局未显示相关性。
Bendardaf等[12]发现,贝伐珠单抗的靶点VEGF-A水平在左半结肠和直肠癌高于右半结肠癌。如果左半结肠和直肠起源肿瘤更具有VEGF-A依赖性,则可以解释肿瘤原发这些部位的患者采用抗VEGF抑制剂治疗后生存改善。右半结肠癌更常见超突变(微卫星不稳定性)、过度甲基化(CpG岛甲基化表型)、BRAF突变以及BRAF突变样基因表达[10,11,16]。这些改变可能存在预后和预测价值,如BRAF(BRAF样)突变和抗-EGFR治疗。但其与抗VEGF治疗的相关性尚未有研究报道。在本研究中,本应纠正BRAF突变对治疗的影响,但因仅少数患者可获得其BRAF突变状态,故未进行。
生存结局的差异中OS较PFS更显著。这可以用一线后续治疗中贝伐珠单抗的使用频率(25%患者)得以解释。此外,根据既定评效标准(如本研究中所采用RECIST)确定疾病进展时,其进展的幅度和严重程度可能存在显著差异。因此,疾病进展时间往往不能作为生存分析的合适替代指标[17]。既然剔除接受后续西妥昔单抗或伊立替康治疗的患者后并未显著改变研究结果,所以这些药物引起的疗效差异不能作为OS显著差异的主要解释。
有关原发肿瘤部位与贝伐珠单抗疗效的前瞻性临床研究的数据目前并未公开,但已有比较直肠癌与结肠癌的报道。III期临床研究AVF2107g显示贝伐珠单抗联合5-Fu和伊立替康(IFL)能改善患者生存,且直肠癌患者(HR0.47)较结肠癌患者(HR0.74)获益更明显,中位OS分别为24.2月和19.5月,而安慰剂组中不同肿瘤原发部位OS相似[5,18]。
研究疗效与安全性的观察性研究BRiTE,将贝伐珠单抗与不同的化疗方案联合,观察到直肠癌与结肠癌患者中位OS差异显著,分别为29.2月和21.9月[19]。AVEX研究中,转移性结肠癌患者随机接受一线卡培他滨+贝伐珠单抗或卡培他滨单药治疗。该研究最近公布的一项亚组分析数据也显示,与结肠癌患者(HR0.67)相比,贝伐珠单抗使直肠癌(HR0.41)和直肠+结肠癌患者(0.22)PFS改善更显著[20]。随机III期临床研究中接受不含贝伐珠单抗的联合化疗方案的结直肠癌患者研究原发肿瘤部位的预后价值,未见结肠与直肠癌患者生存差异的报道[4,6,21-24]。与前面提到的前瞻性研究数据一致,我们观察到当贝伐珠单抗联合化疗时,直肠癌患者较结肠癌患者OS显著延长,而在仅接受联合化疗者未观察到生存差异。
在解释我们研究结果的需要考虑一些重要局限之处。本研究为回顾性研究,而回顾性收集数据可能导致偏倚和数据质量低。本研究未复阅CT扫描结果,从而增加了进展时间判定的不准确性。尽管如此,由于OS并不受这些不确定性的影响,而其也表现出与PFS相同的预后差异,所以这些不确定性不太可能对研究结果有明显影响。剔除数据缺失病例也未对结果产生显著影响。由于接受CAPEOX方案治疗的队列为贝伐珠单抗获批应用之前,与接受CAPEOXBEV方案队列并非在同一时间段,所以两队列的可比性有所下降。此外,两队列的基线变量特征也并不平衡。鉴于此,我们在后续的单一队列和合并队列研究中都进行了多因素分析来纠正这些变量的影响。由于仅接受化疗组的病例数显著少于接受贝伐珠单抗治疗组,所以必然削弱该队列研究结果的可信度。
另一方面,我们观察到的生存结果差异显著,不太可能为偶然事件。此外,已发表的研究化疗±贝伐珠单抗对比直肠癌与结肠癌患者疗效的随机和观察性研究结果也支持原发肿瘤部位与贝伐珠单抗疗效有关[4-6,18-24]。贝伐珠单抗联合CAPEOX方案用于转移性结直肠癌患者一线治疗可能主要使原发肿瘤位于直肠和乙状结肠的患者获益。其他针对VEGF的靶向药物,如阿卜西普和瑞格非尼也可能表现出与原发肿瘤部位相关的疗效差别,所有我们希望靶向药物研究者能进行不同肿瘤原发部位的分层分析。由本研究为回顾性的探索研究,该研究结果仅能视为一假设理论,需要完整的随机试验数据进行验证。














