Nature:PD-1全球研发格局分析
11月4日,最新发表在Nature Reviews Drug Discovery上的一份报告分析了PD-1/PD-L1抗体临床试验的全球现状:3000项临床试验、295个联合靶点、中国招募患者最容易。
PD-1/PD-L1抗体已成为10多种癌症的标准治疗,目前全球有9款这类抗体获批上市,包括帕博利珠单抗, 纳武利尤单抗,Atezolizumab, Avelumab, Durvalumab, Cemiplimab, Toripalimab(拓益), Sintilimab(达伯舒)以及卡瑞利珠单抗(Camrelizumab,艾瑞卡),且仍大量的临床试验正在评估PD-1/PD-L1抗体作为单药或联合用药的其他治疗潜力。

报告指出,自2006年以来,业界共启动了3362项评估PD-1/PD-L1抗体(包括单独用药和联合用药)的临床试验。截至2019年9月,共有2975项临床试验仍然活跃,这些试验累计计划招募50多万名患者。与2017年9月进行的一次调查相比,此次调查结果新增了1469项活跃的临床试验。
报告还显示,目前,有76%活跃的临床试验在测试PD-1/PD-L1抗体与其它癌症疗法(如IO疗法、靶向疗法、化疗或放疗)的联合方案。在过去两年里,最常见的三种联合方案是:与化疗联合,与CTLA-4抗体联合以及与靶向VEGF或其受体VEGFR的疗法联合。
这些临床试验已推动一些联合治疗方案获批,如帕博利珠单抗+Axitinib以及Avelumab+Axitinib治疗肾癌,帕博利珠单抗+Lenvatinib治疗子宫内膜癌,Atezolizumab+Bevacizumab+化疗治疗非小细胞肺癌。
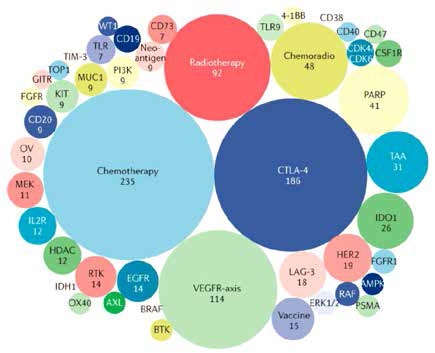
从靶点来看,目前有295个药物靶点被用于与PD-1/PD-L1抗体联合,与2017年的分析相比,增加了136个。最常见的联合靶点包括CTLA-4、VEGF或其受体VEGFR、PARP、IDO1、HDAC、EGFR、HER2、LAG-3、MEK、CD20。
在试验设计方面,报告发现,过去6年里,PD-1/PD-L1抗体临床试验平均计划招募患者数量在下降:从“2014年平均每项试验招募429人”下降到了“2019年平均每项试验招募129人”。试验规模的缩小与针对主要癌症类型(如黑色素瘤、乳腺癌、肾癌以及肺癌)的新试验数量下降有关。相比前几年,最近新增的试验更多的是针对罕见的癌症类型,因此,符合招募条件的患者数量要少得多。
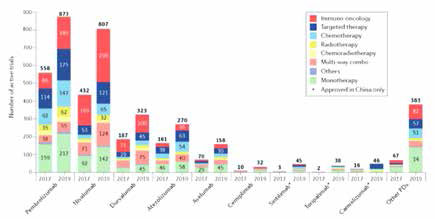
在患者招募方面,报告显示,在中国开展的临床试验的患者招募率最高,这与我国每年新增400多万癌症病例,且大多数患者未能获得PD-1/PD-L1抗体治疗有关。
在结论部分,报告提出了PD-1/PD-L1抗体研发未来需要重视和解决的两个问题:1)随着该领域转向联合治疗,有必要为每种联合治疗策略开发有效的生物标志物,以鉴定可响应这些治疗的患者;2)由于大多数接受现有PD-1/PD-L1抗体治疗方案的患者出现了耐药或复发,因此,该领域应更多关注针对PD-1/PD-L1耐药性的新联合方案的开发。
最后,报告强调,不管是开发新的生物标志物,还是新的治疗方案,都需要开展新的临床试验,而新兴市场大量的可用患者有望支持更快的招募,最终为全世界更多的患者带来更有效的PD-1/PD-L1疗法。
(编译 于晶晶)














