CheckMate-816研究 首个肺癌免疫治疗新辅助治疗研究公布
在近期召开的美国癌症研究协会(AACR)年会上,全球首个肺癌免疫治疗联合化疗新辅助治疗Ⅲ期临床研究CheckMate-816的首个阳性终点结果公布,纳武利尤单抗+化疗的新辅助治疗方案,在肿瘤病理完全缓解(pCR)率上显著优于标准含铂双药化疗。
该研究是首个证实免疫治疗联合化疗新辅助治疗能为可切除NSCLC患者带来pCR显著改善的Ⅲ期临床研究,为降低可切除NSCLC患者术后复发风险、改善患者生存带来新希望。
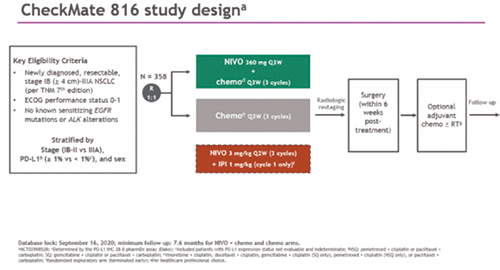
Checkmate-816是一项随机、开放标签、多中心的Ⅲ期临床研究,旨在评估纳武利尤单抗联合化疗用于可切除NSCLC患者新辅助治疗的疗效和安全性。研究纳入358例患者,术前随机接受纳武利尤单抗360 mg联合含铂双药化疗(每3周一次,最多3个周期),或者单用含铂双药化疗(每3周一次,最多3个周期)。
主要研究终点为由盲态独立评审委员会(BIRC)评估的pCR和无事件生存期(EFS),次要终点包括由BIRC评估的主要病理缓解(MPR)、总生存期(OS)以及至死亡或远处转移的时间。探索性终点包括由BIRC评估的客观缓解率(ORR)以及PD-L1等预测性生物标志物。
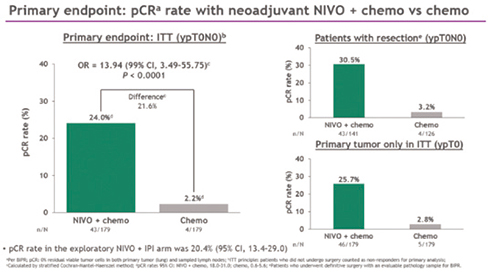
研究结果显示,术前接受纳武利尤单抗联合化疗组的pCR率达24%,而单用化疗组仅为2.2%(OR=13.94,99%CI 3.49~55.75,P<0.0001)。
亚组分析显示,无论患者疾病分期、组织学类型、肿瘤突变负荷(TMB)和PD-L1表达水平如何,纳武利尤单抗联合化疗均可改善pCR。
在次要终点方面,纳武利尤单抗+化疗组的主要病理缓解(MPR)率是单用化疗组的4倍(36.9% vs. 8.9%)。在接受手术切除的患者中,纳武利尤单抗+化疗组的MPR率显著高于单用化疗组(46.8% vs. 12.7%)。
纳武利尤单抗+化疗组的ORR也得到改善,达到54%,单用化疗组为37%。经影像学评估降期的患者,纳武利尤单抗+化疗组和单用化疗组的ORR分别为31%和24%。
纳武利尤单抗+化疗组的ctDNA清除率显著高于单用化疗组(56% vs. 34%)。分析两组ctDNA清除和未清除患者的pCR率发现,ctDNA清除与pCR有关。
安全性方面,纳武利尤单抗+化疗组和单用化疗组的3~4级治疗相关不良事件的发生率分别为34%和37%。纳武利尤单抗+化疗组未发生治疗相关死亡。
研究结果表明,纳武利尤单抗联合化疗新辅助治疗可以给可切除NSCLC患者带来显著的pCR的改善,且在不同分期、不同组织学类型、TMB和PD-L1表达的患者中表现出一致的获益,MPR和ORR均有改善,联合治疗的耐受性良好。
该研究为可切除NSCLC患者的新辅助治疗提供了新的选择,另一主要终点EFS的最终结果值得期待。未来对新辅助免疫治疗的方案、手术时机、疗效评估体系、预测标志物等问题值得进一步研究探讨。
对于免疫新辅助治疗副作用是否会影响手术时机或手术切除率、切除范围和并发症风险等的担忧,从目前的数据来看,纳武利尤单抗各项研究中,超90%的患者完成新辅助治疗,这些患者接受手术切除的比例也接近90%。只有极少数患者因治疗副作用无法手术或耽搁手术。纳武利尤单抗新辅助治疗对手术方式、切除范围、术中并发症和术后死亡风险都没有明显影响,整体治疗是相当安全可控的。
(编译 余军)














