转移性去势抵抗性前列腺癌合并骨转移 177Lu-PSMA-I&T联合223Ra安全可行
澳大利亚Peter MacCallum癌症中心Kostos等报告,在转移性去势抵抗性前列腺癌合并骨转移患者中,镥-177 [177Lu]Lu-PSMA-I&T(177Lu-PSMA-I&T)联合趋骨性α放射性核素镭-223(223Ra)方案是安全且可行的。这一发现支持进一步评估α放射性核素与β放射性核素药物的联合方案。(Lancet Oncol. 2025年10月18日在线版)
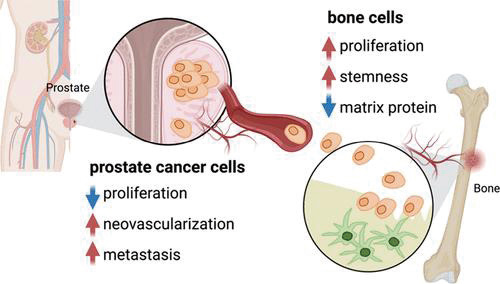
177Lu-PSMA-I&T以及223Ra已被确立为延长转移性去势抵抗性前列腺癌患者生存期的治疗方法;然而,耐药和疾病进展是不可避免的。为了评估177Lu-PSMA-I&T联合223Ra在该患者群体中的安全性及初步抗肿瘤活性,该项研究者发起的单中心、单臂Ⅰ/Ⅱ期临床试验(AlphaBet)在澳大利亚Peter MacCallum癌症中心开展。
入组条件:患者年龄≥18岁;确诊为进展性、转移性去势抵抗性前列腺癌;ECOG PS评分为0~2分;至少有两个未接受放疗的可见的骨转移灶;曾接受雄激素受体通路抑制剂治疗,且前列腺特异性膜抗原(PSMA)阳性(定义为病灶的最大标准化摄取值≥20),并且无不一致的病灶。
Ⅰ期剂量递增阶段评估了两种223Ra剂量水平(27.5 kBq/kg和55.0 kBq/kg),联合静脉应用177Lu-PSMA-I&T(7.4 GBq,每6周一次,最多6个周期)。Ⅱ期剂量扩展阶段继续使用推荐Ⅱ期剂量。共同主要终点为最大耐受剂量或给药剂量,及推荐Ⅱ期剂量(Ⅰ期)以及PSA缓解率(Ⅱ期),分析包括在任一阶段接受最大耐受剂量或给药剂量的全部患者。
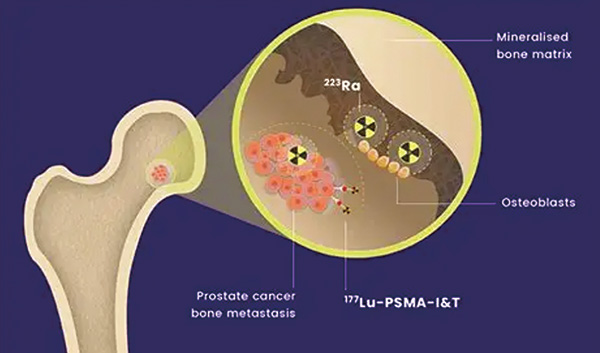
结果显示,2022年11月3日至2024年11月5日,研究共纳入37例患者,其中36例(中位72.5岁)被纳入安全性分析,33例被纳入初步疗效分析。研究未观察到剂量限制性毒性。223Ra的推荐Ⅱ期剂量为55.0 KBq/kg,同时联合7.4 GBq 177Lu-PSMA-I&T,每6周一次。
中位随访13.3个月(IQR:8.7~17.1个月),11例(31%)患者完成了两种给药全部6个周期的治疗。18例(50%)提前终止治疗,主要原因为明确的疾病进展(11例,61%)或不良事件(3例,17%)。18例(55%,95%CI 36%~72%)的PSA降幅至少为50%。36例患者中有5例(14%)出现≥3级治疗相关不良事件,包括贫血(4例,11%)和中性粒细胞减少(3例,8%),但无治疗相关死亡。10例(28%)患者发生无临床意义的3级淋巴细胞减少。
(编译 王磊)














