研究发现放疗与不良预后基因突变有关
美国、德国和荷兰研究者在《自然·遗传学》杂志上发表了放疗与肿瘤基因组之间的相互作用的研究结果。研究发现,放疗可致肿瘤基因突变,以小片段缺失为主要表现,且高突变负荷提示不良预后。(Nat Genet. 2021, 53: 1088-1096. DOI: 10.1038/s41588-021-00874-3)
放疗治疗原理是电离辐射损伤DNA,如造成DNA双链断裂(DSB),DNA损伤如不及时修复则可导致细胞死亡。如修复机制出问题,影响后续DNA复制,亦可导致细胞死亡。
DSB可触发DNA修复途径,包括无错的同源重组(HR),及3种易出错通路:经典非同源端部链接(c-NHEJ)、替代端链接(a-EJ)、单链退火(SSA)。DNA修复过程中产生的错误可能改变肿瘤基因组,测序可检测出这些基因突变。这些基因突变可能预示治疗有效,也可能提示肿瘤耐药(对放疗不敏感)。
研究者观察到,在接受烷化剂治疗的患者肿瘤中出现大量突变,这种现象在替莫唑胺治疗胶质瘤中较为明显。类似现象在放疗诱发第二原发肿瘤(放疗远期不良反应,于放疗结束多年后发生,包括白血病和实体瘤等)中亦可见到,如突增的微小片段缺失突变。
研究发现,放疗与缺失突变增加有显著关联,根治性放疗和姑息性放疗均可增加肿瘤小片段缺失突变负荷,且该关联不受肿瘤MSI和HRD状态影响。姑息放疗患者的肿瘤突变负荷介于未放疗及根治性放疗之间,提示放疗所致的突变负荷增加与放疗剂量相关。放疗所致的片段缺失长度多介于5~15 bp,根治放疗中缺失片段长度较姑息放疗长,该现象可能与放疗剂量有关。对于IDH突变的胶质瘤患者基因分析显示,放疗所致的基因缺失突变为随机分布,并不局限于某个特定位点。
通过GLASS数据库中放疗前后IDH突变的胶质瘤基因组对比,研究者发现放疗后ID8类型突变量显著上升(ID8及下文的ID6均为插入/缺失突变的不同类型)。单碱基替换(SBS)也是放疗后肿瘤突变标志。除了小片段缺失突变,放疗还能造成其他类型的基因突变。GLASS序列患者中,放疗后肿瘤中可见大片段缺失突变(>20 bp),与未放疗肿瘤样本差异显著,放疗后肿瘤中基因倒置错位亦明显增加。
生存分析显示,CDKN2A纯合性缺失突变较CDKN2A野生型预后差。低非整倍体突变负荷的肿瘤患者预后较好,具有高非整倍体突变负荷的肿瘤患者预后差。获得性CDKN2A纯合性突变可作为复发后放疗不敏感的标志物。复发患者的临床评估应包含CDKN2A基因突变检测。
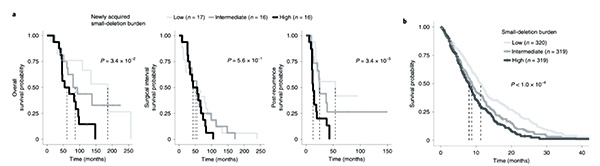
除了CDKN2A纯合性缺失之外,GLASS序列患者中,小片段缺失突变负荷高的肿瘤患者预后明显较负荷低的患者差,且与放疗剂量相关。而对HMF中放疗后的样本分析显示,具有小片段缺失突变水平高的患者的预后较差。
将生存期分为术后至放疗开始的间隔期以及放疗后的生存期分析发现,生存差异仅局限在放疗后的生存期,术后至放疗开始的间隔期则不同片段缺失突变负荷组间无明显差异。
研究者推测,胶质瘤患者可能从初次放疗中获益均等,但放疗所致的基因突变可使部分肿瘤对放疗敏感度下降,导致最终预后出现明显差异。高突变负荷可能提示肿瘤细胞内DNA修复过程活跃,肿瘤细胞死亡减少,表现为放疗疗效不佳。
该研究提示,放疗在治疗作用外,可因其治疗原理导致部分基因突变,某些基因突变反而可降低放疗疗效、导致不良预后。某些放疗相关基因突变可能是预测复发肿瘤对放疗敏感性的标志物,也为开发新的放疗增敏剂提供了参考。 (编译 赵佳)














