免疫组合疗法获批用于NSCLC一线治疗
日前,罗氏(Roche)旗下基因泰克 (Genentech)公司宣布,美国FDA批准该公司的Atezolizumab(Tecentriq)与贝伐珠单抗、紫杉醇和卡铂的组合疗法(ABCP),作为转移性非鳞非小细胞肺癌(NSCLC)患者一线治疗,患者肿瘤不携带EGFR/ALK基因变异。而此前刚授予Atezolizumab优先审评资格,治疗广泛期小细胞肺癌(ES-SCLC)。(自FDA)
根据美国癌症协会的估计,在2018年美国有234 000例新确诊的肺癌患者。肺癌可以分为两大类,非小细胞肺癌和小细胞肺癌。非小细胞肺癌占肺癌总数的85%。
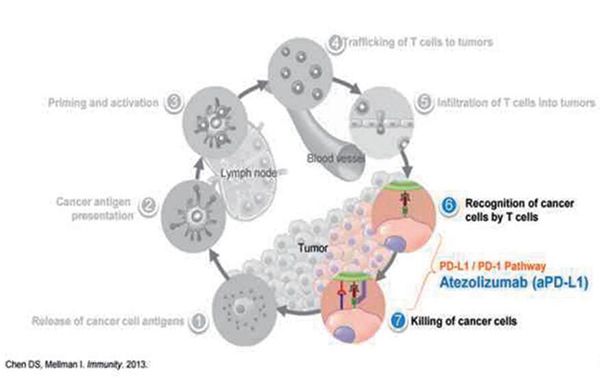
Atezolizumab是罗氏开发的抗PD-L1抗体,通过阻断PD-L1与PD-1和B7.1受体相结合,可重新激活T细胞,促使其杀伤肿瘤细胞。Atezolizumab已获得FDA批准作为治疗转移性NSCLC患者的二线治疗,新的批准将进一步扩大Atezolizumab的适用患者群。
这一批准是基于名为IMpower150的Ⅲ期临床试验结果,该研究中,NSCLC患者接受了ABCP组合疗法,或贝伐珠单抗与化疗(BCP)组合疗法治疗。结果表明,ABCP组合疗法,在野生型意向治疗(ITT-WT)人群中,与BCP组相比,可降低22%的死亡风险。ABCP组中位总生存期为19.2个月,显著优于BCP组的14.7个月(HR=0.78,P=0.016)。ABCP组无进展生存(HR=0.71,P=0.0002)、总缓解率(55% vs. 42%)和缓解持续时间(10.8个月 vs. 6.5个月)均有优势。
罗氏公司相关负责人表示,基于Atezolizumab的组合疗法作为治疗转移性非鳞NSCLC的一线治疗,能显著改善患者生存期。这一适应证批准支持使用Atezolizumab组合疗法治疗肺癌的策略。
Atezolizumab在多种类型肿瘤中显示治疗潜力。截至目前,Atezolizumab已获全球80多个国家批准,用于含铂化疗期间或之后疾病进展且不存在EGFR或ALK基因突变的转移性NSCLC患者,用于不适合接受顺铂化疗或接受含铂化疗期间或之后疾病进展的局部晚期或转移性尿路上皮癌患者。肺癌方面,罗氏正开展9项Ⅲ期研究,评估Atezolizumab单药及与其他药物联合用药的治疗潜力。
(编译 谭新)