复发/难治性非霍奇金淋巴瘤/CLL CAR T细胞疗法再次应用仍有效

美国宾州大学Abramson癌症中心Svoboda等报告,嵌合抗原受体(CAR) T细胞疗法治疗后癌症复发的患者,CAR T细胞疗法再次应用仍有效。(2022 ASH年会.摘要号2016)
CAR T细胞疗法在过去十年中彻底改变了血液系统恶性肿瘤的治疗,为那些已经用尽传统治疗方法的患者提供了希望,但癌症复发或对CAR T细胞疗法不再应答的患者在进一步治疗方面的选择有限。
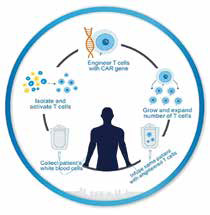
该项正在进行的Ⅰ期临床试验评估了一种新出现的第四代CAR T细胞疗法(huCART19-IL18),用于CD19阳性复发/难治性非霍奇金淋巴瘤或慢性淋巴细胞白血病(CLL)患者,这些患者曾接受了至少两种疗法,包括CAR T细胞疗法。该研究是美国首次使用抗CD19 CAR T细胞联合分泌白细胞介素18(IL-18)的临床试验。
早期结果表明,这种联合方法是安全的,与其他市售可用的CAR T细胞疗法相比,不会导致新的或增加的不良事件。该研究正在继续增加huCART19-IL18的剂量,并将一次招募一例患者,直到确定合适的剂量。
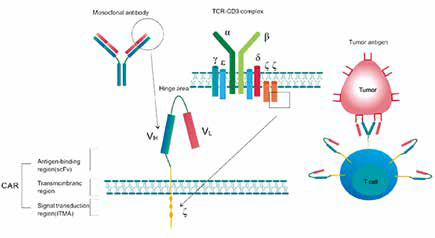
在接受huCART19-IL18治疗的前7例患者中,包括那些之前对市售CAR T细胞疗法没有反应或在治疗后复发的患者,所有患者都对治疗有反应,其中4例完全缓解,3例部分缓解。在第3个月时,4例完全缓解患者均未见疾病复发,并且所有患者在中位8个月的随访中仍生存。
huCART19-IL18相关的毒性事件是暂时的,与其他CAR T细胞产品的毒性相似。4例患者出现细胞因子释放综合征,2例出现神经毒性。未见4级不良事件或研究相关死亡。
值得注意的是,由于生产时间为3天,huCART19-IL18比其他CAR T细胞产品可以更快地进行给药,而其他CAR T细胞产品的常规生产时间为9~14天,这对患有侵袭性快速增长疾病的患者而言尤其重要。之前的一项临床前研究发现,制造时间的缩短也可能增强T细胞的潜能。
(编译 张馨月)