2015ESMO结直肠癌指南更新解读
中山大学附属肿瘤医院 陈功
欧洲肿瘤内科学会(ESMO)结直肠癌诊疗指南一直保持不断更新,与时俱进,同时也更结合临床实践。就在我们逐渐熟悉和应用2014年ESMO结直肠癌诊断指南时,基于结直肠癌领域临床研究的更新和治疗理念的调整,2015版ESMO晚期/转移性结直肠癌指南再次进行了更新。本文从新版指南更新要点看其对诊疗策略与临床实践将产生的影响,以期阐明结直肠癌治疗思路,优化整体治疗策略。
背景:ESMO晚期/转移性结直肠癌(mCRC)诊疗指南的特征
在过去的十年,是我国肿瘤临床治疗开启基于指南的循证医学之路的十年,标志性事件是2005年NCCN(美国国家癌症综合网络)走进中国。结直肠癌的诊疗也不例外,NCCN结直肠癌指南成为业界同行必备的参考书,也是国内卫生部诊疗规范的重要参考。相较而言,ESMO结直肠癌相关指南走进中国学者的视界,则是大约5年后的2010年左右了。ESMO结直肠癌相关指南共分4册:3册诊断治疗与随访指南(早期结肠癌、转移性结直肠癌和直肠癌)及1册结直肠癌家族性风险指南;ESMO 的诊治指南修订有其独特的形式,一般是先形成“共识指南”(consensus guideline),然后经广泛讨论后再最终成文为“临床诊治指南”(clinical practice guideline),因此与NCCN指南相比,期更新频率较慢,一般1-2年更新一次。
近年来,ESMO指南在结直肠癌诊治方面提出了很多与NCCN指南不同的新观念和新策略,得到了越来越多的业界同行的认可,其中最受瞩目的当属直肠癌诊疗指南(基于高分辨率MRI[核磁共振]局部复发危险度分层的局部进展期直肠癌分层治疗策略)以及mCRC诊疗指南,尤其后者,开创性的提出mCRC患者分组,以转移瘤是否可手术切除为核心,联合考虑疾病进展的快慢以及患者对治疗的耐受及需求,而将患者分成不同的治疗组别(组0至组3),分别适用不同的治疗目标、治疗策略和治疗方法,详见表-1;开创了基于治疗目标的晚期结直肠癌个体化治疗的新篇章,迅速得到业界的认可,并成为mCRC的标准诊治策略,也让 ESMO mCRC指南得到全球业界的广泛接受和认可,包括我国的同道。
那么,2015年更新的mCRC指南,其核心内容是什么?与2014版相比,又改变了什么?
框架及结构的重要改变
旧版的患者4分组法(表-1)是指南的核心,分组的标准既考虑疾病因素(肿瘤分布、生物学行为),也考虑患者身体因素(能否耐受高强度治疗),新版指南改变的显著特点就是摒弃传统的患者4分组法,而从疾病特征和患者状况两个维度进行分类。
改变1:疾病分类代替患者分组
这也许是2015版指南最大的改变,我个人认为这是理念、策略上的重要改变。
1. 不再使用传统的分组方法
在2015年7月西班牙巴塞罗那召开的WCGIC(世界胃肠肿瘤大会)上,指南执笔人van Cutsem教授代表指南写作专家组介绍新指南时,着重提出,新版指南将不再沿用旧版的将mCRC患者分为4组的做法(表-1),原因就是在临床实践中,组1和组2,以及组2和组3之间没有明确的界限,临床很难分开,不具有可操作性。因为分组的主要依据,除了转移瘤可切除性这个核心标准(甄别组0与其他组别)外,还纳入了肿瘤进展快慢、肿瘤相关症状等因素(甄别组2和组3),而后面这两个因素主要是肿瘤生物学行为的外在体现,从而使得临床界定变得异常困难,因为,目前尚未有公认的标准在肿瘤初诊时对其生物学行为做出准确预判。这也是传统ESMO患者分组的局限之处。

2. 将mCRC分为两大类:局限性mCRC和广泛性mCRC
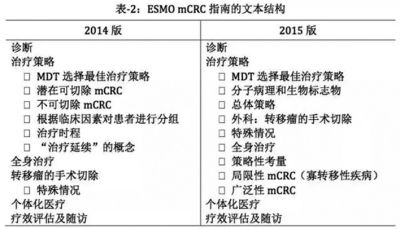
2014版和2015版mCRCESMO指南的文本结构见表-2。在2015版指南中,将mCRC疾病分为两大类:oligometastatic disease(OMD,寡转移性疾病)和metastatic disease(转移性疾病)。我个人理解为局限性和广泛性mCRC。
这里出现了一个新名词,寡转移(OMD); OMD是近几年在肿瘤学领域新兴的一个名词,与中文“寡”对应的“孤立”意思并不同的是,肿瘤学领域的寡转移,业界的定义一般指转移灶数目少于5个的特殊时期,其含义是指肿瘤转移过程中的一种中间状态,它是介于局限性原发瘤及广泛性转移瘤之间生物侵袭性较温和的阶段。从定义上可以看出来,OMD代表的是一个疾病解剖学或组织上的分布状态,是相对客观的、容易界定的。
寡转移治疗的关键是放疗、手术和射频消融等局部治疗,同时兼顾预防远处转移。这个治疗理念与策略对于mCRC尤其重要。在新版指南中,OMD概念的提出就是与包括手术在内的局部治疗手段捆绑在一起,这揭示了两方面的信息:一,局部治疗是OMD治疗策略中的重要组成部分,能为显著延长患者生存,甚至带来治愈机会;局部治疗方法中手术切除是最主要的,其在mCRC治疗中的价值已经在过去的20多年实践里得到验证,广为接受,但不仅限于此,近几年来,其他各种局部消融毁损技术(射频消融、微波消融、冷冻消融等)、立体定向放疗、放射性元素标记的局部内放疗等对于局限性mCRC的治疗价值越来越得到肯定;二,按治疗方法可以对疾病进行分类。按照是否可手术切除,过去我们将mCRC分为“可/适合切除”和“不可/适合切除”mCRC,相信以后将会变为“可/适合局部治疗”mCRC和“不可/适合局部治疗”mCRC,2015版ESMO指南的变化,就是一个信号。
由上可见,新版ESMO指南用“疾病分类”来取代“患者分组”,一方面更加客观,临床实践中更具可操作性,另一方面,新的疾病分类对治疗目标和临床治疗策略具有更强的指向性:局限性mCRC治疗目标是达到治愈意向的无瘤状态(NED),更要考虑局部治疗,而广泛性mCRC则更要以全身治疗为主,主要目标是疾病控制。
遗憾的是,ESMO指南中并没有对OMD进行详细阐述,因此,指南中何为局限性何为广泛性疾病,是不是以5个转移瘤为标准?并不是十分清晰。
改变2:患者状况分类
新版指南更加强调患者本身因素,根据年龄、体力状态、器官功能及合并症等情况将其分为临床适合(fit)和不适合(unfit)两类,且在这两类之间还存在临床不适合但能仍从临床治疗中获益的中间类别,继而根据患者分组制定后续诊疗策略。对于Fit/Unfit的标准,尽管指南里是以身体状况为标准,但我个人认为也要考虑其他情况,比如因为经济状况、家庭支持、医保状况、医疗资源/治疗手段的可获得性等,因为临床实践中这些因素明显的制约着治疗决策。
严格来说,将患者按是否“适合”高强度临床治疗分类并不是新的改变,在既往版本指南中已经出现,只是,既往的患者4组分组法将疾病状态和患者身体状态混在一起,而新指南中将其独立出来,不考虑疾病状态,只单纯从身体状况这一维度来看是否适合按照疾病分类拟给予的治疗方案。而且2015版指南将身体状况分类作为治疗决策中第一个考虑的问题,优先于疾病分类,能让后续制定的治疗方案更加贴近临床和患者及家庭状况,临床上更具可实践性。在既往指南中,推荐的考量顺序是首选根据疾病分类拟定治疗方案,然后再来考虑患者是否能耐受/适合治疗。
这一小小的改变,尽管没有改变肿瘤的疾病性质,但却对临床治疗决策起到了很现实的作用,这也更加体现了现代肿瘤治疗中的“以人为本”、“治疗的应该是患肿瘤的病人而不是病人身上的肿瘤”这一核心理念。
指南要点:基于治疗目标的初始治疗决策
2015年新版指南依旧维持了四个治疗目标:达到NED(无瘤状态)或治愈;缩瘤或转化;疾病控制;最佳支持;分别对应临床适合的各疾病状态分类患者及临床不适合患者,但在某些具体细节上,还是有了一些变化。这也是指南里关于治疗策略与方法描述最详尽的部分。
下面将重点内容详细分析
1. 局限性mCRC(OMD)
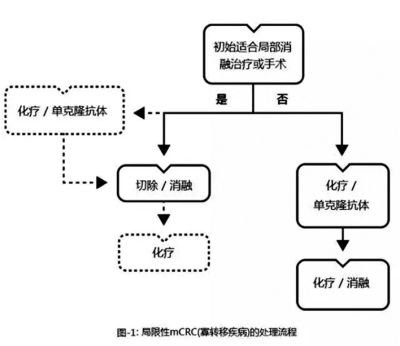
该类疾病的整体处理思路及流程详见图-1;核心是选择最佳的围手术(或局部治疗)期治疗方案。所有患者首选应该面临的问题就是“是否适合进行初始手术/局部治疗”?并依此而进行后续的相关治疗,详见下述。
需要强调的是,新版指南中一旦将疾病归为局限性mCRC(OMD),即意味着患者的治疗目标将是通过手术/局部治疗±全身化疗达到NED,除非是在进行局部治疗前疾病已经进展为广泛期疾病。也许这正是2015版ESMO指南将该类疾病单列的重要意义所在:只要肿瘤转移局限,均应积极争取根治。
1)初始可切除者
a) 治疗目标:维持NED,争取治愈
b) 治疗策略/方法:手术+围手术期化疗(术前新辅助和/或术后辅助)
对于该疾病分组的初始治疗,可以直接手术,也可以参照EPOC研究的治疗模式(FOLFOX术前新辅助化疗+肝切除手术),在旧版指南中,推荐大多数情况下采用新辅助治疗模式,2015指南中专家组意识到EPOC研究的治疗模式已经不再是唯一的,很多情况下也适用直接手术。
此种情况下,指南里比较一致的推荐是对于术前未接受化疗且无既往治疗的NED(切缘干净)患者给予辅助治疗。
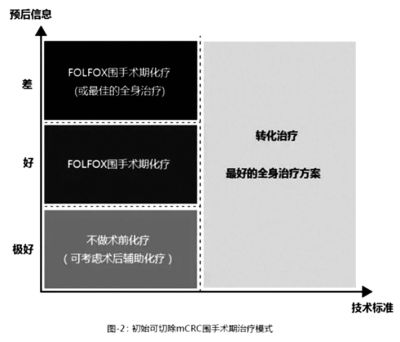
而对于围手术期治疗模式的选择,2015版指南做了比较大的更改,明确提出要从“手术技术标准”和“肿瘤学预后因素”两个维度进行考量(图-2),其中手术技术分为“容易切除”和“困难切除”两个标准,肿瘤学预后信息则分为“极好”“好”和“差”三个标准,主要衡量参数涉及肿瘤生物学行为,尽管指南认为尚没有明确的评判指标,我个人认为目前最好的还是复发风险评分的五个参数:转移瘤数目、大小、转移瘤出现的时间、原治疗目标发瘤区域淋巴结是否转移及血CEA(癌胚抗原)水平。总体来说,越容易切除、预后越好的肿瘤越不需要围手术化疗,尤其是术前化疗;反之,切除越困难、预后越差的患者,不但需要术前化疗,而且化疗方案的强度也应增强,而不仅仅局限在FOLFOX(图-2)。
2)初始不可切除者
a) 治疗目标:缩小肿瘤,争取转化
b) 治疗策略/方法:最强烈的全身治疗方案
具体的治疗推荐与旧版指南一致,根据肿瘤的RAS基因状态来决定,野生型患者,两药化疗(FOLFOX或FOLFIRI)联合EGFR单抗(西妥昔单抗或帕尼单抗)是治疗的首选,也可以考虑FOLFOXIRI±贝伐单抗;RAS突变型患者,推荐FOLFOXIRI±贝伐单抗,或两药化疗。
3)OMD中局部治疗手段的应用
对于所有的OMD患者,除了手术以外,均应考虑积极的局部治疗,可以和手术联合使用,例如,为了减少手术创伤,手术切除较大的肝脏转移瘤后,对于小的、深在的肝转移瘤配合术中RFA(射频消融),已经成为临床上普遍采用的一种治疗模式;如因伴发病、估计残余器官功能不足或其他因素而无法手术的OMD,更应积极应用各种局部治疗手段来配合全身化疗。
常用的非手术局部治疗手段包括:各种消融术(射频、微波、冷冻等)、立体定向放疗(SBRT)、高剂量近距离放疗、放射性栓塞治疗等。
2. 广泛性mCRC:
1)以疾病控制(disease control)为治疗目标的临床适合患者:
a)推荐的一线治疗是:化疗+贝伐单抗,或化疗+EGFR单抗(RAS野生型)。
b)每2-3月评估一次肿瘤情况,只要有证据显示疾病得到控制,就应该继续治疗;
c)在2次肿瘤评估后,如果疾病仍然得到控制,应该考虑进行有效的维持治疗。
该类别的一线治疗推荐,2015版指南中对两类单抗的靶向治疗并无优先推荐顺序之分别。这是较2014版有所改变,旧版中“综合考虑各种因素,主要是整体治疗规划、毒副反应、患者意愿等,最常推荐的是贝伐单抗”。
2015新版指南继续推荐维持治疗策略,并首次做出更加详细的指引(更多信息见下“维持治疗”)。
2)以细胞减灭(cytoreduction)为治疗目标的临床适合患者:
a)如果肿瘤为潜在可切除:RAS野生型患者应该接受两药化疗+EGFR单抗治疗;RAS突变型则优先推荐三药化疗(或两药)±贝伐单抗;
b)疗效最佳时进行肿瘤评估(通常在治疗后3-4个月),一旦出现肿瘤退缩,应考虑行潜在根治性的手术切除和/或消融治疗来消灭所有病灶,达到NED状态;
c)如果第一次肿瘤评估未见治疗应答,两药细胞毒化疗方案应该更换以争取手术切除的最大机会;一旦出现疾病进展,应该更换为二线治疗;
3)维持治疗的规约:
a)诱导化疗为FOLFOX或CAPOX时,应在化疗3-4月后转入维持治疗;
b)诱导化疗为FOLFIRI时,应该持续治疗直至不再出现肿瘤退缩或肿瘤已经达到稳定化状态;
c)5-FU/卡培他滨或+贝伐单抗(推荐)应维持治疗直到疾病进展;
d)含贝伐单抗的诱导化疗后,最佳维持治疗方案是氟化嘧啶类+贝伐单抗;不推荐贝伐单抗单药进行维持治疗。
e)维持治疗全过程中,均可以考虑初始诱导化疗的再引入。
2015版ESMO指南是首次对维持治疗做出了如此详尽的规约,说明在ESMO框架内已经广泛接受了这一治疗理念,尽管ESMO指南直到2014年才推荐“维持治疗”这一理念;相较而言,NCCN指南虽然早在2007年就提出“维持治疗”的概念,但直到今天,也没有对这一策略做出如此详尽的规约。在维持治疗已经作为临床新常态的今天,相信2015 ESMO指南关于维持治疗的上述规约,将具有很好的临床指导意义。
3. 基于分子标志物的个体化治疗
1)推荐对所有患者均行RAS、BRAF等基因状态测定以便提供最佳诊断、预后及治疗决策,RAS的内容详见上述。
2)BRAF突变:根据既往临床研究数据,BRAF突变型患者的总生存期(OS)更短,接受后续治疗的比例更低,这部分患者的预后极差。因此,指南建议在一线治疗中给予高强度的治疗方案。近期TRIBE研究的亚组分析显示,三药化疗+贝伐珠单抗能给BRAF突变的患者带来生存获益;既往OPUS研究与CRYSTAL研究的联合分析结果也表明,BRAF突变mCRC仍然能从表皮生长因子受体(EGFR)抑制剂西妥昔单抗的治疗中获益。因此,尽管两个研究病例数都非常有限,但在BRAF突变型患者治疗中,三药化疗+贝伐珠单抗和双药化疗+抗EGFR单抗也许就是指南中提及的“高强度治疗”,我个人认为应属可选方案。
临床实践中如何很好地实施指南
1. 明确改善mCRC生存的关键因素
a)提高一线治疗的疗效- 个体化选择最佳治疗
b)创造“治愈的机会”- 转移灶的手术切除(和其他局部毁损性治疗)
c)采用“治疗的延续”-整体规划、优化选择,在不同线数的治疗中使用最佳疗法
2.基于问题的初始治疗(一线)决策模式
a)患者临床上是否适合接受标准治疗?
◎ Fit / Unfit
b)患者的治疗目标是什么?
所有涉及临床适合患者的治疗决策,必须由MDT根据相应的分子分析来制定
c)患者需要哪一种治疗强度的化疗方案?
◎ 单药化疗+/- Bev
◎ 两药化疗+/-抗EGFR单抗(RAS野生型)或贝伐单抗
◎ 三药化疗+/-Bev
d)应该结合分子分型来决定最佳的全身治疗方案
结语
综上所述,2015版ESMO指南在疾病分类方面做出了重大调整,目的是有助于辨识局限性mCRC患者群体,对潜在可治愈患者进行积极干预;在具体治疗策略及方法方面,2015指南并没有太多更新,核心还是基于疾病分类和治疗目标的临床决策,优化mCRC整体治疗策略;在具体临床实践中,首先将患者根据身体状况分为“适合”与“不适合”,更是体现了“以人为本”的现代肿瘤治疗理念;深刻理解、学习和实践2015 ESMO指南,必定有助于mCRC临床治疗的优化,最终改善患者的生存。














